- m3.comトップ
- > DI Station
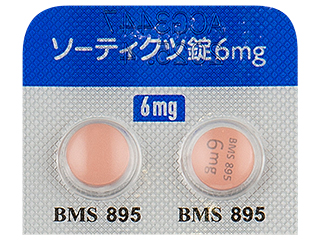
- > ソーティクツ錠6mg

警告
-
1.1 本剤は結核等の感染症を含む緊急時に十分に対応できる医療施設、あるいは当該医療施設との連携下において、本剤についての十分な知識と適応疾患の治療に十分な知識・経験をもつ医師のもとで、本剤による治療の有益性が危険性を上回ると判断される症例のみに使用すること。本剤は感染症のリスクを増大させる可能性があり、また結核の既往歴を有する患者では結核を活動化させる可能性がある。また、本剤との関連性は明らかではないが、悪性腫瘍の発現が報告されている。治療開始に先立ち、本剤が疾病を完治させる薬剤でないことも含め、本剤の有効性及び危険性を患者に十分説明し、患者が理解したことを確認した上で治療を開始すること。[2.1、2.2、8.1、8.2、8.6、9.1.1、9.1.2、11.1.1、15.1.2参照]
-
1.2 重篤な感染症
-
ウイルス、細菌等による重篤な感染症が報告されているため、十分な観察を行うなど感染症の発症に注意し、本剤投与後に感染症の徴候又は症状があらわれた場合には、直ちに担当医に連絡するよう患者を指導すること。[2.1、8.1、9.1.1、11.1.1参照]
-
-
1.3 本剤の治療を開始する前に、光線療法を含む既存の全身療法(生物製剤を除く)の適用を十分に勘案すること。[5.参照]
禁忌
-
2.1 重篤な感染症の患者[症状を悪化させるおそれがある][1.1、1.2、8.1、9.1.1、11.1.1参照]
-
2.2 活動性結核の患者[症状を悪化させるおそれがある][1.1、8.2、9.1.1、9.1.2参照]
-
2.3 本剤の成分に対し過敏症の既往歴のある患者
効能・効果
-
既存治療で効果不十分な下記疾患
-
尋常性乾癬、膿疱性乾癬、乾癬性紅皮症
-
用法・容量
-
通常、成人にはデュークラバシチニブとして1回6mgを1日1回経口投与する。
注意事項
重要な基本的注意
-
8.1 本剤は、感染のリスクを増大させる可能性があるので、本剤の投与に際しては、十分な観察を行い、感染症の発症や増悪に注意すること。感染症の徴候又は症状があらわれた場合には、速やかに担当医に連絡するよう患者を指導すること。[1.1、1.2、2.1、9.1.1、11.1.1参照]
-
8.2 本剤投与に先立って結核に関する十分な問診及び胸部X線検査に加えてインターフェロンγ遊離試験又はツベルクリン反応検査を行い、適宜胸部CT検査等を行うことにより、結核感染の有無を確認すること。また、本剤投与中も、胸部X線検査等の適切な検査を定期的に行うなど結核の発現には十分に注意し、結核を疑う症状(持続する咳、体重減少、発熱等)が発現した場合には速やかに担当医に連絡するよう患者を指導すること。なお、結核の活動性が確認された場合は結核の治療を優先し、本剤を投与しないこと。[1.1、2.2、9.1.2参照]
-
8.3 帯状疱疹等のウイルスの再活性化が報告されていることから、ヘルペスウイルス等の再活性化の徴候や症状の発現が認められた場合には、患者に受診するよう説明し、本剤の投与を中断し速やかに適切な処置を行うこと。また、ヘルペスウイルス以外のウイルスの再活性化にも注意すること。
-
8.4 本剤投与によるB型肝炎ウイルスの再活性化のおそれがあるので、投与に先立ってB型肝炎ウイルス感染の有無を確認すること。[9.1.3参照]
-
8.5 本剤投与中は生ワクチン接種による感染症発現のリスクを否定できないため、生ワクチン接種を行わないこと。
-
8.6 臨床試験において皮膚及び皮膚以外の悪性腫瘍の発現が報告されている。本剤との因果関係は明確ではないが、悪性腫瘍の発現には注意すること。[1.1、15.1.2参照]
慎重投与
-
9.1 合併症・既往歴等のある患者
-
9.1.1 感染症(重篤な感染症又は活動性結核を除く)の患者、感染症が疑われる患者又は再発性感染症の既往歴のある患者
-
感染症を悪化又は顕在化させるおそれがある。[1.1、1.2、2.1、2.2、8.1、11.1.1参照]
-
-
9.1.2 結核の既往歴を有する患者又は結核感染が疑われる患者[1.1、2.2、8.2参照]
-
(1)結核の既往歴を有する患者では、結核を活動化させるおそれがある。
-
(2)結核の既往歴を有する場合又は結核感染が疑われる場合には、結核の診療経験がある医師に相談すること。下記のいずれかの患者には、原則として本剤の投与開始前に適切な抗結核薬を投与すること。
-
・胸部画像検査で陳旧性結核に合致するか推定される陰影を有する患者
-
・結核の治療歴(肺外結核を含む)を有する患者
-
・インターフェロンγ遊離試験やツベルクリン反応検査等の検査により、既感染が強く疑われる患者
-
・結核患者との濃厚接触歴を有する患者
-
-
-
9.1.3 B型肝炎ウイルスキャリアの患者又は既往感染者(HBs抗原陰性、かつHBc抗体又はHBs抗体陽性)
-
肝機能検査値やHBV DNAのモニタリングを行うなど、B型肝炎ウイルスの再活性化の徴候や症状の発現に注意すること。[8.4参照]
-
-
-
9.3 肝機能障害患者
-
9.3.1 重度の肝機能障害(Child-Pugh分類C)のある患者
-
可能な限り投与を避けること。やむを得ず投与する場合には、患者の状態をより慎重に観察し、副作用の発現に十分注意すること。本剤非結合形の血中濃度が上昇し、副作用が強くあらわれるおそれがある。[16.6.2参照]
-
-
-
9.5 妊婦
-
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。ラットで単回投与後にデュークラバシチニブ又はその代謝物は母動物の胎盤及び羊膜嚢に移行したが、胎児では検出されなかった。胚・胎児発生に関する試験において、AUC比較で臨床曝露量の約266倍(ラット)及び約20倍(遊離血清中濃度、ウサギ)に相当する最高投与量まで、胚致死作用及び催奇形性は認められていない。
-
-
9.6 授乳婦
-
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)において、デュークラバシチニブ又はその代謝物が乳汁中へ移行することが認められている(乳汁中濃度/血漿中濃度比:2.7〜30.9)
。動物実験(ラット)における妊娠及び哺育期間中の投与により、AUC比較で臨床曝露量の約110倍に相当する投与量で、離乳前の期間に出生児の一過性の体重減少が認められている。
-
-
9.7 小児等
-
小児等を対象とした臨床試験は実施していない。
-
過量投与
-
13.1 処置
-
循環血液中のデュークラバシチニブは透析によりほとんど除去されない。[16.6.1参照]
-
適用上の注意
-
14.1 薬剤交付時の注意
-
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
-
その他の注意
-
15.1 臨床使用に基づく情報
-
15.1.1 免疫抑制剤又は光線療法と併用した場合の安全性及び有効性は確立していない。
-
15.1.2 国際共同第III相臨床試験(IM011-046試験)と海外第III相臨床試験(IM011-047試験)の統合解析において投与0〜52週に本剤投与群(969人・年)でリンパ腫1例を含む悪性腫瘍(非黒色腫皮膚癌を除く)が0.2%(0.3/100人・年)に報告された。この発現率は、一般的な乾癬患者やレジストリで報告されている悪性腫瘍(非黒色腫皮膚癌を除く)の発現率(0.4〜2.3/100人・年)と同程度であった
。悪性腫瘍の発現における本剤との関連性は明らかではない。[1.1、8.6参照]
-
相互作用
副作用
重大な副作用及び副作用用語
重大な副作用
-
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
-
11.1.1 重篤な感染症(0.2%)
-
ウイルス、細菌等による重篤な感染症があらわれることがある。本剤投与中に重篤な感染症を発現した場合は、感染症が消失するまで本剤の投与を中止すること。[1.1、1.2、2.1、8.1、9.1.1参照]
-
その他の副作用
-
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
| 5%以上 | 1〜5%未満 | 1%未満 | |
| 感染症及び寄生虫症 | 上気道感染 | 単純ヘルペス | 帯状疱疹 |
| 胃腸障害 | 口腔潰瘍 | ||
| 皮膚及び皮下組織障害 | ざ瘡様皮疹 | 毛包炎 | |
| 臨床検査 | 血中CK増加 |
薬価
ソーティクツ錠6mg 2533.4円/錠
m3.comにご登録済の方
薬剤名検索
薬剤情報提供:一般財団法人日本医薬情報センター 剤形写真提供:株式会社薬事日報社
・薬剤情報・剤形写真は月一回更新しておりますが、ご覧いただいた時点で最新情報ではない可能性がございます。 最新情報は、各製薬会社のWebサイトなどでご確認ください。
・投稿内容の中に適応外、承認用法・用量外の記載等が含まれる場合がありますが、エムスリー、製薬会社が推奨するものではありません。

 同薬効薬剤
同薬効薬剤
