- m3.comトップ
- > DI Station
- > 消化器官用薬
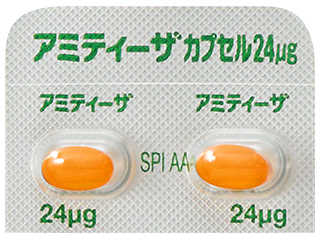
- > アミティーザカプセル24μg

禁忌
-
腫瘍,ヘルニア等による腸閉塞が確認されている又は疑われる患者[腸閉塞を悪化させるおそれがある.]
-
本剤の成分に対し過敏症の既往歴のある患者
-
妊婦又は妊娠している可能性のある婦人[「妊婦,産婦,授乳婦等への投与」の項参照]
効能・効果
-
慢性便秘症(器質的疾患による便秘を除く)
用法・容量
-
通常,成人にはルビプロストンとして1回24μgを1日2回,朝食後及び夕食後に経口投与する.なお,症状により適宜減量する.
注意事項
重要な基本的注意
-
動物実験で胎児喪失が報告されているので,妊娠する可能性のある婦人に投与する場合には妊娠検査を行うなど妊娠中でないことを確認すること.また,本剤の妊娠に及ぼす危険性について患者に十分に説明し,服薬中は避妊させること.なお,本剤投与中に妊娠が確認された場合又は疑われた場合には,直ちに医師に連絡するよう,指導すること.
慎重投与
-
中等度又は重度の肝機能障害のある患者[本剤又は活性代謝物の血中濃度が上昇するおそれがある(「用法・用量に関連する使用上の注意」,「薬物動態」の項参照).]
-
重度の腎機能障害のある患者[本剤又は活性代謝物の血中濃度が上昇するおそれがある(「用法・用量に関連する使用上の注意」,「薬物動態」の項参照).]
適用上の注意
-
薬剤交付時
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること.[PTPシートの誤飲により,硬い鋭角部が食道粘膜へ刺入し,更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することが報告されている.]
その他の注意
-
ラットに本剤20,100及び400μg/kg/日投与(体表面積換算で臨床用量の4,20及び81倍)を2年間投与したがん原性試験において,400μg/kg/日を投与した雄ラットで精巣の間質細胞腺腫の発生率が有意に増加した.雌ラットでは肝細胞腺腫の用量依存的な発生頻度増加がみられた.
-
ラットの受胎能及び着床までの初期胚発生に関する試験において,対照群に対し,本剤1000μg/kg/日投与(体表面積換算で臨床用量の約166倍)で着床数及び生存胎児数の有意な減少がみられた.
相互作用
副作用
副作用発現状況の概要
-
承認時における安全性評価対象例(1日48μg投与例)315例中,196例(62%)に臨床検査値異常を含む副作用が認められた.主な副作用は下痢95例(30%),悪心73例(23%)等であった.
その他の副作用
-
以下のような副作用が認められた場合には症状に応じて,減量又は中止するなど,適切な処置を行うこと.
| 5%以上 | 1〜5%未満 | 1%未満 | 頻度不明※ | |
| 血液及びリンパ系障害 | 貧血 | |||
| 免疫系障害 | 気道過敏症 | |||
| 代謝及び栄養障害 | 食欲減退 | |||
| 神経系障害 | 頭痛 | 浮動性めまい,体位性めまい,感覚鈍麻,傾眠,失神 | ||
| 耳及び迷路障害 | 回転性めまい | |||
| 心臓障害 | 動悸 | 頻脈 | ||
| 血管障害 | ほてり | 低血圧 | ||
| 呼吸器,胸郭及び縦隔障害 | 呼吸困難 | 咳嗽 | ||
| 胃腸障害 | 下痢(30%),悪心(23%),腹痛(6%) | 腹部不快感,腹部膨満,嘔吐 | 消化不良,排便回数増加,出血性胃炎,痔核,逆流性食道炎,心窩部不快感,痔出血 | |
| 皮膚及び皮下組織障害 | 湿疹,紅斑 | 発疹 | ||
| 筋骨格系及び結合組織障害 | 背部痛,筋骨格硬直,四肢不快感 | |||
| 全身障害及び局所様態 | 胸部不快感(5%) | 胸痛,不快感,異常感(気分不良),倦怠感,浮腫,口渇 | ||
| 臨床検査 | 血中ビリルビン増加,血中クレアチンホスホキナーゼ増加,血中ブドウ糖増加,血中トリグリセリド増加,血中尿素増加,血中γ-グルタミルトランスフェラーゼ増加,尿中ブドウ糖陽性,ヘモグロビン減少,体重増加,白血球数増加,血中リン増加 | 血圧低下 |
-
※自発報告において認められている副作用のため頻度不明.
薬価
アミティーザカプセル24μg 123円/カプセル
m3.comにご登録済の方
薬剤名検索
薬剤情報提供:一般財団法人日本医薬情報センター 剤形写真提供:株式会社薬事日報社
・薬剤情報・剤形写真は月一回更新しておりますが、ご覧いただいた時点で最新情報ではない可能性がございます。 最新情報は、各製薬会社のWebサイトなどでご確認ください。
・投稿内容の中に適応外、承認用法・用量外の記載等が含まれる場合がありますが、エムスリー、製薬会社が推奨するものではありません。

 同薬効薬剤
同薬効薬剤

副作用の頻度
投稿日: 2015/02/20 参考率: 94%(225人/239人)
内科/60代/処方経験あり